Марганцовокислый калий
Содержание:
- Приготовление раствора
- При беременности
- Взаимодействие
- Внутреннее применение
- Методика спринцевания влагалища
- Раствор марганцовки для обработки ран
- Кислый привкус во рту
- Профилактика диабета с помощью марганца
- Горький привкус во рту
- Когда нужно использовать
- Применение марганцового раствора на ранах
- Внимание!
- Фармакологические свойства
- Передозировка
- Химические свойства
- Получение
- Физические свойства
- Инструменты для спринцевания влагалища
- Цена Марганцовки. Где взять Перманганат калия?
- Марганец и мышечные рефлексы
- Достоинства и недостатки
- Марганец и витамины
Приготовление раствора
Что нужно знать, чтобы правильно развести марганцовку для лечебных целей?
Необходимо запомнить, что для 1% раствора марганцовки понадобится 1 г кристаллов марганцовки и 100 г воды. Обыкновенная чайная ложка имеет объем 5 мл. Если насыпать в нее марганцовку и убрать ножом горку, получится 6 г кристаллов. Из этого количества марганцовки для приготовления 1% раствора понадобится 600 мл воды.
1% раствор марганцовки имеет практически черный окрас. Это очень крепкий раствор. Его не применяют для внутреннего потребления во избежание ожогов слизистой. 1% раствор используют для лечения грибковых заболеваний, бородавок, пролежней. Такой раствор оказывает подсушивающее и местно-раздражающее действие, значительно ускоряющие процессы кровообращения.
Для приготовления слабых растворов берут меньшее количество кристаллов марганцовки.
Для приготовления растворов нельзя использовать металлические ёмкости, иначе это химическое вещество вступит в контакт с металлом, что станет причиной потери некоторой части лекарственных свойств и, кроме этого оставит несмываемые следы на посуде. Стеклянные ёмкости лучше всего подходят для приготовления растворов из марганцовки.
Воду для приготовления раствора надо брать теплую кипяченую. В теплой воде растворение кристаллов происходит намного лучше. Проводить полоскания и промывания также гораздо комфортнее тёплым раствором.
Кристаллы марганцовки не следует брать руками, так как можно получить ожог и оставить на коже некрасивые плохо смываемые следы. Взять несколько кристалликов поможет спичка или кончик ножа.
Полученный раствор обязательно профильтруйте через марлю, сложенную в несколько слоев, чтобы нерастворившиеся кристаллики не попали на слизистые или кожу и не стали причиной ожога.
При приготовлении раствора сначала в ёмкость наливают необходимое количество воды, а затем добавляют сухие кристаллы марганцовки.
Раствор перманганата калия сохраняет лечебные свойства в течение нескольких часов после приготовления. Как только жидкость примет коричневую окраску использовать его не имеет смысла: все полезные свойства утеряны.
Крепкий раствор марганцовки при длительном применении может стать причиной ожогов кожи.
Хранить кристаллы марганцовки следует в тёмном, сухом месте в плотно закрытой упаковке или ёмкости.
При беременности
При беременности допускается только наружное применение марганцовки. Прием раствора перманганата калия внутрь противопоказан.
Определение беременности при помощи Марганцовки
Этот метод определения беременности относится к категории “бабушкиных”, однако многие беременные женщины утверждают, что он является достаточно точным.
В 500 л теплой воды разводят небольшое количество порошка перманганата калия (чтобы жидкость окрасилась в бледно-розовый цвет) и добавляют к полученному раствору немного мочи.
Если жидкость светлеет, беременности нет, если на дно банки выпал осадок в виде хлопьев — есть основания предполагать беременность.
Взаимодействие
Марганцовокислый калий химически несовместим с рядом органических веществ (включая танин, сахар, уголь).
Взрывается при обработке концентрированной H2SО4 (серной кислотой).
Даже при незначительном (до комнатной температуры) нагреве активно взаимодействует с большинством восстановителей (например, с глицерином) и легкоокисляющимися веществами. Реакция сопровождается саморазогреванием, что в ряде случаев вызывает самовоспламеняющиеся смеси и может привести к взрыву.
Очень опасно растирать кристаллы марганцовокислого калия с порошками активных металлов и неметаллов (алюминием, серой, кальцием, фосфором, магнием и др.), поскольку подобные действия нередко сопровождаются взрывом.
Внутреннее применение
Для внутреннего применения перманганата калия раствор показан только при острых отравлениях. Его эффективность в этом случае объясняется тем, что во время контакта жидкости с белками, производимыми человеческим организмом, выделяется активный кислород. Он является грозой микробов. Таким образом, при попадании раствора марганцовки в органы пищеварения происходит процесс перехода опасных химических веществ в неопасную форму.
Дополнительно полезна в случае острого отравления ещё одна особенность марганцовокислого калия – его специфический запах. Благодаря этому можно значительно быстрее и легче вызвать рвоту с целью очищения желудка. После того как раствор будет выпит, не следует спешить с очищением желудка. Лучше какое-то время дать ему проявить своё действие.
Для промывания желудка необходимо приготовить очень слабый раствор марганцовки, где отношение действующего вещества к воде составляет от 0,01:100 до 0,1:100. На практике трудно сохранить точные пропорции, но можно ориентироваться на такие факторы, как количество крупинок и цвет. На литр кипячёной воды обычно берут 3-4 кристалла перманганата калия. Если ориентироваться по окрасу раствора, то после растворения порошка жидкость должна быть бледно-розовой.
Методика спринцевания влагалища
У спринцевания влагалища есть свой алгоритм выполнения процедуры. Заключается он в следующем:
Женщина занимает положение лежа на гинекологическом кресле или кушетке, которые застелены клеенкой и чистой пеленкой или простыней. Снизу под таз подставляется специальное судно, в которое будет стекать раствор. Если делается горячее спринцевание, то судно не нужно, так как при использовании наконечника Морозова или промывателя Пинкуса жидкость по трубке сливается прямо в ведро
После того, как пациентка заняла надлежащую позицию, акушерка осторожно вводит наконечник кружки или другого инструмента во влагалище, снимает зажим с резиновой трубки и жидкость начинает поступать внутрь. Кружку при этом удерживают на высоте около метра над уровнем живота женщины.
С особой осторожностью необходимо проводить спринцевание влагалища девушкам, не имевшим половых контактов, так как имеется шанс повредить девственную плеву. При проведении процедуры таким пациенткам пластиковый наконечник заменяется на резиновый катетер, а раствор вводится под небольшим напором.. Стоит отметить некоторые моменты, при которых спринцевание влагалища не делается
К ним относятся: беременность, менструация, первые несколько дней после родов или аборта. К тому же не надо забывать, что частые промывания могут нарушить естественную микрофлору влагалища, а это уже грозит быстрым размножением патогенных микроорганизмов и, как следствие различного рода осложнениями. Поэтому любое спринцевание, даже если оно лечебное, не должно проводиться без консультации и назначения гинеколога.
Стоит отметить некоторые моменты, при которых спринцевание влагалища не делается. К ним относятся: беременность, менструация, первые несколько дней после родов или аборта. К тому же не надо забывать, что частые промывания могут нарушить естественную микрофлору влагалища, а это уже грозит быстрым размножением патогенных микроорганизмов и, как следствие различного рода осложнениями. Поэтому любое спринцевание, даже если оно лечебное, не должно проводиться без консультации и назначения гинеколога.
Также хотелось бы развеять некоторые мифы по поводу спринцевания влагалища как способа предотвратить наступление беременности или защитить от инфекций, передающихся половым путем. Гинекологами всего мира научно доказано, что ни один раствор не снижает риск нежелательного зачатия, даже если спринцевание было проведено сразу после полового акта. Что касается инфекционных заболеваний — также не имеется никаких достоверных фактов, что промывание влагалища антисептическими растворами помогут избежать заражения.
Раствор марганцовки для обработки ран
Он выступает в роли антисептика, оказывающего мощное действие при поражениях кожного покрова. Следует отметить, что при разной степени повреждения раствор может меняться, то есть, если они незначительны, то достаточно будет применить слабый состав, а при более же серьезных — отлично подойдет пятипроцентная лечебная жидкость.
Как сделать 5% раствор марганцовки:
- Возьмите 5 гр. перманганата калия, всыпьте в 100 мл теплой кипяченой воды.
- После того как все кристаллы растворяться полученную жидкость следует тщательно процедить через сложенную в несколько слоев марлю, дабы избежать попадания на кожный покров не растворившихся кристаллов.
- Готовый состав должен иметь характерный насыщено-фиолетовый оттенок и использоваться в охлажденном виде, исключительно для наружного применения. В данном случае ранок, которые следует обрабатывать лишь у их краев, в противном случае можно лишь занести инфекцию.
Кислый привкус во рту
Кислота во рту – симптом повышенной кислотности в желудке. Кислый привкус дает желудочный сок – биологическая жидкость, необходимая для полноценного пищеварения. При нарушениях питания, например, при злоупотреблении копченостями или жирной пищей, вырабатывается излишек кислоты. Так желудок стремится переварить тяжелую пищу. Также кислота активно вырабатывается в ответ на специи и раздражающие продукты.
При повышенной кислотности разрушается слизистая оболочка желудка и пищевода, в ответ начинается воспаление – гастрит, эзофагит. На поврежденных участках образуются эрозии и язвы. Диагноз почти очевиден, если вкус кислоты усиливается ночью и утром или во время активных физических нагрузок. Это чувство также сопровождается тяжестью и болью в груди, изжогой и отрыжкой. В случае язвы почти всегда возникают жжение в пищеводе и частая отрыжка.
Жжение в пищеводе
Повышение кислотности в желудке сопровождается жжением в пищеводе, тошнотой, рвотой, запорами и изжогой.
Ещё одна причина кислого привкуса – гастроэзофагеальный рефлюкс – процесс, при котором кислотное содержимое желудка поднимается в пищевод. В этом случае кислота очень жгучая и насыщенная.
Если вы не только чувствуете кислотность во рту, но и замечаете, что на языке образовался налет, это может указывать на начало грибковой инфекции. Это часто происходит после лечения антибиотиками, из-за диабета или при ослаблении иммунной системы.
При появлении кислого вкуса во рту, нужно обратиться к гастроэнтерологу. Возможно, нужно будет сдать желудочный сок на анализ и пройти гастроскопию. Ожидая назначение лечения, нужно изменить свой рацион, избегая жирной пищи, выбирая легкоусвояемые продукты. Не переедайте, предпочитайте есть меньшими порциями чаще. Грибковые инфекции лечат только медикаментами.
Профилактика диабета с помощью марганца
Согласно многим теориям, благодаря марганцу можно проводить прекрасную профилактику сахарного диабета – он тормозит это коварное заболевание, не дает ему развиваться. Заболеваний щитовидной железы тоже было бы намного меньше, если бы люди принимали марганец в достаточных количествах.
Марганец влияет на работу сердечно-сосудистой системы, обмен инсулина. Научные исследования доказывают, что в организме человека, который болен сахарным диабетом, марганца становится меньше в два раза, чем у тех, кто этим заболеванием не страдает. Это происходит по причине того, что марганец нужен для переработки сахара. Если человек болен сахарным диабетом, ему нужно принимать марганец в увеличенных количествах – можно как добавку, а можно в комплексе с другими добавками, витаминно-минеральными.
Горький привкус во рту
Горечь – четкий сигнал о проблемах в пищеварительной системе. Горький привкус дает желчь при нарушении работы желчных протоков, желчного пузыря или печени. Когда эти органы функционируют нормально, желчь, протекая по желчевыводящим протокам, беспрепятственно поступает в двенадцатиперстную кишку. При нарушении их работы она может попадать в пищеварительную систему.
Горький привкус во рту
Так бывает при холецистите и камнях в желчном пузыре. В этом случае пациента беспокоит целый ряд симптомов: горький привкус обычно сопровождается болью под ребрами с правой стороны и частой тошнотой, тремором, лихорадкой, потерей аппетита, рвотой.
Длительный прием лекарств
Если вы чувствуете горечь во рту, запишитесь на УЗИ брюшной полости для проверки состояния печени и желчного пузыря. Также нужно сдать биохимический анализ крови, обнаруживающий ферменты печени. В случае тяжелых симптомов выполняют гастроскопию.
До назначения медикаментозного лечения соблюдайте строгую диету, исключив из меню жирные, жареные, маринованные и острые продукты. Скорее всего, гастроэнтеролог назначит прием специальных препаратов – гепатопротекторов, защищающих печень от токсичных веществ и повышающих активность клеток органа.
Когда нужно использовать
Для освобождения желудка от ядовитых соединений рекомендуется использовать воду с небольшим количеством перманганата – вода окрашивается в чуть розоватый цвет. Раны на коже и ожоги лечатся крепким раствором марганцовки. Гнойные образования на ране также обрабатываются сильно концентрированным настоем.
Промывание слизистой желудка требуется, если:
- При отравлении пищей отмечается симптом – тошнота или рвота.
- Требуется избавиться от отравления фальсифицированным алкоголем и дешёвым напитком.
- Развивается интоксикация фосфором либо хинином, синильной кислотой, щелочью.
Человеку с сильной аллергической реакцией на перманганат калия промывать слизистую желудочного тракта нельзя. Возможны побочные эффекты: крапивница и аллергический бронхит или ринит.
Ребёнок и подросток до 18 лет использовать настой должен только по рекомендации лечащего врача. Доза рассчитывается тщательно, чтобы не навредить организму. Грудных детей обычно купают в воде с марганцовкой. Это хорошо обеззараживает и защищает кожу.
Пить раствор для снятия симптомов отравления нельзя. Можно вызвать осложнение в самочувствии пострадавшего. Использование марганца производится чётко по рекомендации врача.
Применение марганцового раствора на ранах
Мало знать, как приготовить раствор марганцовки, необходимо также правильно обрабатывать им раневую поверхность, чтобы исключить негативный эффект. Слабо окрашенная вода обладает антибактериальным свойством и убивает разные вредные микроорганизмы, однако нельзя допускать попадания марганца внутрь раны, поскольку это может привести к обратному эффекту и к возникновению инфекции. Обрабатывать следует только края раны и кожный покров вокруг нее.
При первичной обработке только что появившейся раны, следует внимательно осмотреть ее на наличие инородных тел. Если в рану попала земля, стружка, какие-либо другие загрязнения, то нельзя самостоятельно вытаскивать их, так как можно спровоцировать кровотечение и инфицирование. Перманганат калия также можно использовать во время перевязок, если бинт присох к раневой поверхности. Для того чтоб безболезненно снять повязку и не нарушить образование новых клеток, нужно смочить ее слабым раствором, дождаться, пока бинт размокнет, и отделить от раны.
Внимание!
Для простоты восприятия информации, данная инструкция по применению препарата «Марганец» переведена и изложена в особой форме на основании официальной инструкции по медицинскому применению препарата. Перед применением ознакомьтесь с аннотацией, прилагающейся непосредственно к медицинскому препарату.
Описание предоставлено с ознакомительной целью и не является руководством к самолечению. Необходимость применения данного препарата, назначение схемы лечения, способов и дозы применения препарата определяется исключительно Лечащим врачом. Самолечение опасно для Вашего здоровья.
Фармакологические свойства
Марганцовка – это фиолетовый порошок, в состав которого входят крошечные кристаллы. При смешивании с водой они образуют красный раствор. В медицине данное средство называют перманганатом калия.
Это средство имеет выраженные антисептические свойства. Они связаны с возможностью вырабатывать активный кислород при контакте с органическими элементами – к примеру, белками дермы человека.
Применение марганцовки при интоксикации базируется на способности окислять большинство соединений, имеющих органическое и неорганическое происхождение. Перманганат калия позволяет получить следующие результаты:
В кале появилась желчь: причины и лечение
- Сделать неактивными химические элементы – к ним, в частности, относятся алкогольные напитки и их суррогаты;
- разрушить стенки клеток множества микробов, которые являются причиной интоксикации организма.
Передозировка
Симптомы передозировки проявляются резкой болью в ротовой полости, по ходу пищевода и в животе, диареей, рвотой. Слизистая ротоглотки отекает (возможен отек гортани), изменяет цвет на темно-коричневый или фиолетовый.
Кроме того, у пострадавшего развиваются ожоговый шок и механическая асфиксия; появляются судороги, двигательное возбуждение, явления паркинсонизма, нефропатии, геморрагического колита, гепатопатии.
При пониженной кислотности желудка может развиться метгемоглобинемия с одышкой и выраженным цианозом.
Для ребенка смертельной является доза, равная 3 г. Для взрослого величина смертельной дозы колеблется в пределах от 0,3 до 0,5 г/кг.
Лечение: в/в введение 5% раствора Аскорбиновой кислоты (30 мл), в/м введение Пиридоксина 5% (3 мл) и Цианокобаламина (до 1 г), а также 1% раствора метиленового синего (50 мл).
Химические свойства
| Окисленная форма | Восстановленная форма | Среда | E, В |
|---|---|---|---|
| MnO4− | MnO42− | OH− | +0,56 |
| MnO4− | H2MnO4 | H+ | +1,22 |
| MnO4− | MnO2 | H+ | +1,69 |
| MnO4− | MnO2 | OH− | +0,60 |
| MnO4− | Mn2+ | H+ | +1,51 |

Слева направо (водные растворы): Co(NO3)2 (красный); K2Cr2O7 (оранжевый); K2CrO4 (жёлтый); NiCl2 (бирюзовый); CuSO4 (голубой); KMnO4 (фиолетовый)
Раствор KMnO4 в воде в мерной колбе
Является сильным окислителем. В зависимости от pH раствора окисляет различные вещества, восстанавливаясь до соединений марганца разной степени окисления. В кислой среде — до соединений марганца(II), в нейтральной — до соединений марганца(IV), в сильно щелочной — до соединений марганца(VI). Примеры реакций приведены ниже (на примере взаимодействия с сульфитом калия):
в кислой среде:
- 2KMnO4+5K2SO3+3H2SO4⟶6K2SO4+2MnSO4+3H2O{\displaystyle {\ce {2KMnO4 + 5K2SO3 + 3H2SO4 -> 6K2SO4 + 2MnSO4 + 3H2O}}};
в нейтральной среде:
- 2KMnO4+3K2SO3+H2O⟶3K2SO4+2MnO2+2KOH{\displaystyle {\ce {2KMnO4 + 3K2SO3 + H2O -> 3K2SO4 + 2MnO2 + 2KOH}}};
в щелочной среде:
- 2KMnO4+K2SO3+2KOH⟶K2SO4+2K2MnO4+H2O{\displaystyle {\ce {2KMnO4 + K2SO3 + 2KOH -> K2SO4 + 2K2MnO4 + H2O}}}.
Однако последняя реакция (в щелочной среде) идёт по указанной схеме только при недостатке восстановителя и высокой концентрации щёлочи, которая обеспечивает замедление гидролиза манганата калия.
При соприкосновении с концентрированной серной кислотой перманганат калия взрывается, однако при аккуратном соединении с холодной кислотой реагирует с образованием неустойчивого оксида марганца(VII):
- 2KMnO4+H2SO4⟶K2SO4+Mn2O7+H2O{\displaystyle {\ce {2KMnO4 + H2SO4 -> K2SO4 + Mn2O7 + H2O}}}.
При этом в качестве промежуточного продукта может образовываться интересное соединение — оксосульфат марганца MnO3HSO4{\displaystyle {\ce {MnO3HSO4}}}. По реакции с фторидом иода(V) можно получить аналогичный оксофторид:
- KMnO4+IF5⟶KF+IOF3+MnO3F{\displaystyle {\ce {KMnO4 + IF5 -> KF + IOF3 + MnO3F}}}.
При нагревании разлагается с выделением кислорода (этим способом пользуются в лаборатории для получения чистого кислорода). Схему реакции упрощённо можно представить уравнением:
- 2KMnO4→∘tK2MnO4 +MnO2 +O2{\displaystyle {\ce {2KMnO4->K2MnO4\ +MnO2\ +O2}}}.
На самом деле реакция идёт намного сложнее, например, при не очень сильном нагревании её можно примерно описать уравнением:
- 5KMnO4→∘tK2MnO4 +K3MnO4 +3MnO2 +3O2{\displaystyle {\ce {5KMnO4->K2MnO4\ +K3MnO4\ +3MnO2\ +3O2}}}.
Реагирует с солями двухвалентного марганца, например:
- 2KMnO4+3MnSO4+2H2O⟶5MnO2+K2SO4+2H2SO4{\displaystyle {\ce {2KMnO4 + 3MnSO4 + 2H2O -> 5MnO2 + K2SO4 + 2H2SO4}}}.
Эта реакция в принципе обратна дисмутации (диспропорционирование) K2MnO4{\displaystyle {\ce {K2MnO4}}} на MnO2{\displaystyle {\ce {MnO2}}} и KMnO4{\displaystyle {\ce {KMnO4}}}.
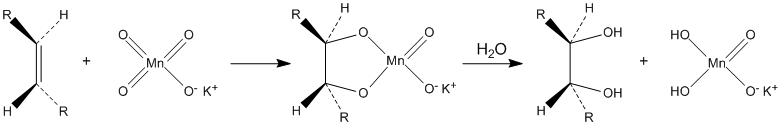
Окисляет органические вещества. В частности, разбавленные растворы перманганата калия в щелочной и нейтральной среде окисляют алкены до диолов (реакция Вагнера):
Водные растворы перманганата калия термодинамически нестабильны, но кинетически довольно устойчивы. Их сохранность резко повышается при хранении в темноте.
При смеси с пероксидом водорода протекает следующая реакция:
- 2KMnO4+3H2O2⟶2MnO2+3O2↑+2H2O+2KOH{\displaystyle {\ce {2KMnO4 +3H2O2 -> 2MnO2 + 3O2 ^ + 2H2O + 2KOH}}}.
Перманганат калия реагирует с концентрированной соляной, бромоводородной или иодоводородной кислотой. В результате выделяются свободные галогены:
- 2KMnO4+16HCl⟶2KCl+2MnCl2+5Cl2↑+8H2O{\displaystyle {\ce {2KMnO4 + 16HCl -> 2KCl + 2MnCl2 + 5Cl2 ^ + 8H2O}}}
Во время химической реакции хлорид-анион Cl−{\displaystyle {\ce {Cl^{-}}}} окисляется до элементарного хлора, а ион Mn7+{\displaystyle {\ce {Mn^{7+}}}} в перманганат-анионе восстанавливается до катиона Mn2+{\displaystyle {\ce {Mn^{2+}}}}:
- 2Cl−⟶Cl2↑{\displaystyle {\ce {2Cl^{-}-> Cl2 ^}}}
- Mn7+⟶Mn2+{\displaystyle {\ce {Mn^{7+}-> Mn^{2+}}}}
Получение
Химическое или электрохимическое окисление соединений марганца, диспропорционирование манганата калия. Например:
- 2MnO2+3Cl2+8KOH→2KMnO4+6KCl+4H2O{\displaystyle {\mathsf {2MnO_{2}+3Cl_{2}+8KOH\rightarrow 2KMnO_{4}+6KCl+4H_{2}O}}}
- 2K2MnO4+Cl2→2KMnO4+2KCl{\displaystyle {\mathsf {2K_{2}MnO_{4}+Cl_{2}\rightarrow 2KMnO_{4}+2KCl}}}
- 3K2MnO4+2H2O→2KMnO4+MnO2+4KOH{\displaystyle {\mathsf {3K_{2}MnO_{4}+2H_{2}O\rightarrow 2KMnO_{4}+MnO_{2}+4KOH}}}
- 2K2MnO4+2H2O→2KMnO4+H2↑+2KOH{\displaystyle {\mathsf {2K_{2}MnO_{4}+2H_{2}O\rightarrow 2KMnO_{4}+H_{2}\uparrow +2KOH}}}
Последняя реакция происходит при электролизе концентрированного раствора манганата калия и эндотермична, она является основным промышленным способом получения перманганата калия.
Физические свойства
Внешний вид: тёмно-фиолетовые кристаллы с металлическим блеском. Показатель преломления составляет 1,59 (при 20 °C).
Растворяется в воде (см. таблицу), жидком аммиаке, ацетоне (2:100), метаноле, пиридине.
| Температура, °C | 10 | 20 | 25 | 30 | 40 | 50 | 65 |
|---|---|---|---|---|---|---|---|
| Растворимость, г/100 г воды | 4,22 | 6,36 | 7,63 | 9 | 12,5 | 16,8 | 25 |
Термодинамические свойства
| Стандартная энтальпия образования ΔH | −813,4 кДж/моль (т) (при 298 К) |
|---|---|
| Стандартная энергия Гиббса образования G | −713,8 кДж/моль (т) (при 298 К) |
| Стандартная энтропия S | 171,71 Дж/(моль·K) (т) (при 298 К) |
| Стандартная мольная теплоёмкость Cp | 119,2 Дж/(моль·K) (т) (при 298 К) |
Инструменты для спринцевания влагалища
Основным инструментом для спринцевания влагалища является кружка Эсмарха. Самая распространенная — это резиновая модель. Но бывают металлические, эмалированные и даже стеклянные кружки. Стеклянные эсмарховские кружки считаются самыми удобными в плане содержания их в чистоте и стерилизации.
Все виды этого инструмента для промывания имеют резиновую трубку, отходящую от емкости с раствором. На трубку надевается наконечник, который может иметь разную форму. Все зависит от задачи, возлагаемой на спринцевание. Если назначено обычное промывание влагалища, то обычно используют кружку Эсмарха.
Для горячего спринцевания, ввиду особенностей процедуры, применяют совсем другой инструментарий. Дело в том, что при горячем спринцевании самое главное — не травмировать ткани вульвы, поэтому необходимо исключить соприкосновение вытекающего из влагалища раствора с кожей. Этого можно добиться, используя наконечник Морозова или промыватель влагалища Пинкуса. Эти медицинские приспособления имеются только в процедурных кабинетах гинекологических отделений, так как требуют специальных навыков в использовании
Поэтому женщинам важно помнить — если врач назначил спринцевание, особенно горячее, то делать его должны только специалисты, а самостоятельное промывание влагалища в домашних условиях может не только не дать ожидаемого результата, но и нанести серьезный вред.
Цена Марганцовки. Где взять Перманганат калия?
Приобрести Перманганат калия непросто. В интернете много как сообщений о том, что марганцовка запрещена и найти ее очень проблематично.
На вопрос, почему запретили продажу этого средства, некоторые фармацевты отвечают, что соответствующими приказами марганцовку приравняли к взрывчатым веществам, и продавать ее без лицензии нельзя.
Другие же говорят, что марганцовокислый калий отнесен к наркотическим веществам и, опять-таки, его продажа без соответствующей лицензии невозможна.
В советах относительно того, где купить марганцовку в аптеке Москвы, обычно указывают специализированные аптеки при родильных отделениях и детских поликлиниках, а также ветеринарные аптеки.
Перманганат калия купить в Москве можно также в хозяйственных магазинах и магазинах, которые реализуют товары для садоводства.
Аналогичные рекомендации дают в ответ на вопрос, где можно купить марганцовокислый калий в СПб или Киеве.
Марганец и мышечные рефлексы
С помощью марганца можно вернуть утраченный тонус мышц или улучшить их состояние. Ноги и руки, которые потеряли чувствительность в результате заболеваний, благодаря марганцу могут вернуть ее.
Марганец останавливает или замедляет развитие остеопороза и артроза. Он помогает сосудам развиваться более активно. Улучшается качество кровотока. Когда человек принимает марганец, в крови становится намного меньше плохого холестерина, кровь лучше сворачивается, она не такая жирная и вязкая, снижается риск образования тромбов.
Вы слышали, как у вас или у ваших знакомых хрустят суставы шеи, пальцев, коленей? Если употреблять в пищу продукты с марганцем, вы избавитесь от этих проблем. Мышцы, кости и сухожилия при включении в рацион этого микроэлемента станут более крепкими, подвижными, будет меньше растяжений и переломов.
Достоинства и недостатки
Преимущества сернокислого марганца:
- препарат длительного пролонгированного действия, накапливается в слоях грунта, постепенно высвобождаются питательные вещества;
- полностью растворяется в воде, легко приготовить раствор в домашних условиях;
- используют на любых типах грунта;
- полностью восполняет дефицит марганца и серы в почвенной микрофлоре;
- подкормка обеспечивает полноценное усвоение азота, фосфора и калия в почве и растениях;
- осеннее внесение подготовит сад и кустарники к морозной зиме;
- весеннее внесение оптимизирует процессы роста и развития;
- рекомендуется использование на солонцах, лесных, песчаных почвах.
Недостатки (скорее, особенности):
соединения серы полноценно усваиваются именно в период вегетации.
в закисленном грунте подвижность марганца снижена, перед внесением важно вносить раскислители (известь, мел);
на черноземах и подзолистых грунтах вносят осторожно, при условии острой нехватки элементов серы и марганца;
важно не перекормить растения, передозировка повышает риск интоксикации
Марганец и витамины
Усвоение витаминов благодаря марганцу происходит быстрее, особенно – витаминов группы В, витамина С, витамин Е. С марганцем быстрее размножаются и развиваются новые клетки организма, с ним быстрее заживают ранки, царапины и другие повреждения кожи. С марганцем быстрее и четче работает мозг и обмен веществ происходит быстрее.
Удивительно, но благодаря марганцу людям удается смягчить приступы остеопороза и остеоартроза, ревматоидного артрита. Марганец способствует тому, что хрящи быстрее растут и становятся крепче – эта функция особенно полезна для детей, подростков и людей, которые перенесли травмы костной ткани. Марганец также активно помогает бороться с катарактой, рассеянным склерозом сетчатки и другими заболеваниями глаз, что особенно полезно для людей, которые теряют зрение, а также пожилых людей.